日期:2013-06-27 来源:本站 供稿: 作者:管理员 类别:摘录转发
定居在人类肠道中的数万亿有害细菌会对人类的健康表现出持续性的威胁,肠道固有的免疫功能可以在我们机体和微生物生态系统之间建立一道保护性屏障,近日,来自北卡罗莱纳大学医学院的研究者通过研究,鉴别出了人类肠道免疫系统发育的基础结构。相关研究刊登于国际杂志Cell Reports上。肠道中特殊的免疫结构,比如肠道相关的淋巴组织(GALT),其是肠道免疫系统的主要组分;当病毒如HIV或者自体免疫障碍如炎性肠病损伤GALT时,肠道免疫功能出现妥协。通过修复损伤的GALT或许可以使得数百万遭受这样疾病的个体获益,开发出相应的疗法就必须对人类GALT有很清楚的理解。
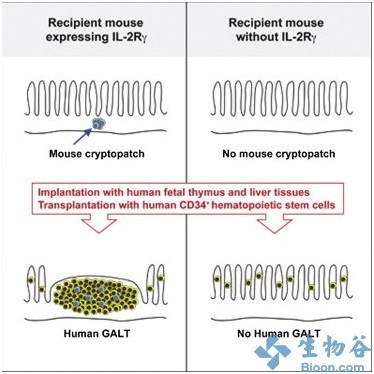
在小鼠中,称为cryptopatches的细胞聚集体是GALT的发育的位点;人类肠道中较小细胞聚集体的存在还具有一定的争议性,研究者使用人化的小鼠揭示了cryptopatches可以作为人类GALT形成的基本物质。在文章中研究者通过生物工程化操作使人类免疫系统分别进入两种密切相关的小鼠品系中(两种小鼠的差别仅仅体现在产生cryptopatches上),当人类机体中cryptopatches存在时,人类的GALT结构就会形成,而且GALT结构可以促进人类的肠道免疫功能,包括产生特异性抗体的功能等。
研究者Paul Denton表示,我们的模型揭示了人类GALT发育的一个新的方面,而且也阐述了肠道免疫系统效应的两个分段过程。而且cryptopatches在人类和小鼠机体中工作的原理似乎是一样的。这项研究证实了,人源化嵌合小鼠机体中可以表现出正常人类免疫系统的功能,而且该研究也提出了许多研究进展,这将帮助推动影响胃肠道功能的研究,下一步研究者将继续使用动物模型来检测这种再生疗法是否可以修复人类机体损伤的GALT。相关研究由NIH等机构提供资助。
来源:生物谷Bioon.com
供稿:国际合作处