日期:2015-08-07 来源:本站 供稿:化学药与医疗器械处 作者:管理员 类别:摘录转发
为了掌握美国FDA否决抗肿瘤新分子实体药物新药上市申请的原因,美国FDA药品评审中心的管理人员系统调查了2005年3月17日到2015年3月17日这十年间,向美国FDA提交的抗肿瘤新分子实体药物新药上市申请的审批情况。对美国FDA否决的抗肿瘤新分子实体药物,详细研究了新药上市申请被拒绝的深层原因,以期对从事抗肿瘤新分子实体药物研发的企业提供参考。
一、2005-2015年抗肿瘤新分子实体药物新药上市申请被否决概况
2005年3月17日到2015年3月17日这十年间,共有15个抗肿瘤新分子实体药物的新药上市申请被否决。根据新药上市申请被否决原因的不同,科研人员将新药分成两大类:1)有效性不足的新药(10个新药,占全部药物的67%);2)临床试验设计存在缺陷的新药(5个新药,占全部药物的33%)。没有药物因为安全性问题而未能通过FDA审批。
表2005-2015年未通过美国FDA审批抗肿瘤新分子实体药物上市申请原因统计
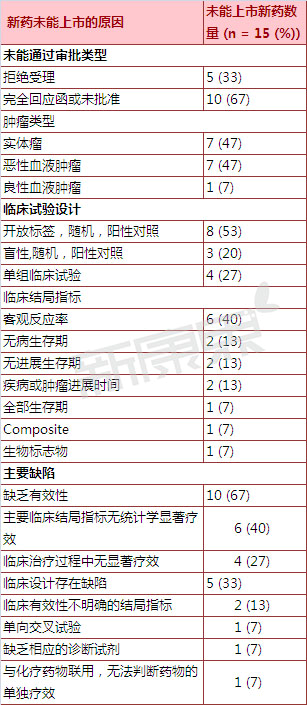
二、10个抗肿瘤新分子实体药物的新药申请因有效性问题而被FDA否决
10个抗肿瘤新分子实体药物的新药上市申请因为有效性问题而被FDA否决,其中6个新药因为主要临床结局指标无统计学显着疗效而被FDA否决,因此申请人如果想获得新药批准,最好针对亚组的数据详细分析结局指标,如从受试者地理分布、病人特点、不同治疗周期等方面分析结局指标的差异。
另外4个新药因临床治疗效果不显着而被FDA否决。其中2个新药开展的随机试验中,尽管治疗效果显着,但是与对照药物相比优势不明显。另外2个新药开展的单组临床试验,由于提供的客观缓解率数据不足以反映临床疗效因此被FDA否决。
三、5个抗肿瘤新分子实体药物的新药申请因临床试验设计存在缺陷而被FDA否决
5个抗肿瘤新分子实体药物的新药申请因临床试验设计存在缺陷而被FDA否决,其中2个新药因采用的临床结局指标不能很好的反映药物的治疗效果而被FDA否决;第3个新药开展的是国际多中心临床试验,采用一线治疗药物为对照。由于在研究该新药对不同国家患者的疗效时采用的是单向交叉试验,因此被FDA认为存在临床设计缺陷而被否决。第4个新药开展的是单组临床试验,纳入的是肿瘤发生特定型突变的患者。但是由于在临床是没有相应的诊断试剂鉴别遴选出相应的肿瘤患者,因此被FDA否决。第5个新药开展的是单独临床试验,在服用完该药后患者继续开展化学治疗,由于不能很好的说明该药的单独疗效因而被FDA否决。
四、小结
抗肿瘤新药的审批总体上来说是一个利益-风险平衡的过程,药监部门需要综合考虑新药的安全性数据、有效性数据、肿瘤的发病率、疾病的危害程度、患者可选择的用药类型、临床对新治疗方法需求的迫切程度等方方面面的因素。对于抗肿瘤新药研发公司来说,了解和掌握药监部门否决相关新药上市申请的原因,设计更加合理完善的临床试验方案和临床结局指标,将有助于提高新药上市申请的批准的可能性。
来源:生物探索