日期:2026-04-30 来源:-- 供稿:国际合作与人才处 作者:-- 类别:独立撰写
生物医学新技术临床研究备案
二、办理范围
本指南适用于已列入《生物医学新技术临床研究备案指导清单》的生物医学新技术,且满足下列要求之一的,以判断其安全性、有效性,明确其适用范围、操作流程、技术要点等的活动,纳入生物医学新技术临床研究范围:
(一)直接对人体进行操作的;
(二)对离体的细胞、组织、器官等进行操作,后植入或者输入人体的;
(三)对人的生殖细胞、合子、胚胎进行操作,后植入人体使其发育的;
(四)国务院卫生健康部门规定的其他方式。
三、办理依据
《生物医学新技术临床研究和临床转化应用管理条例》
国家卫生健康委员会
五、备案条件
按照备案材料目录准备材料,齐全后即可进行申报。申报事项属于本部门职权范围,申报资料真实、准确、完整,符合形式审查要求。
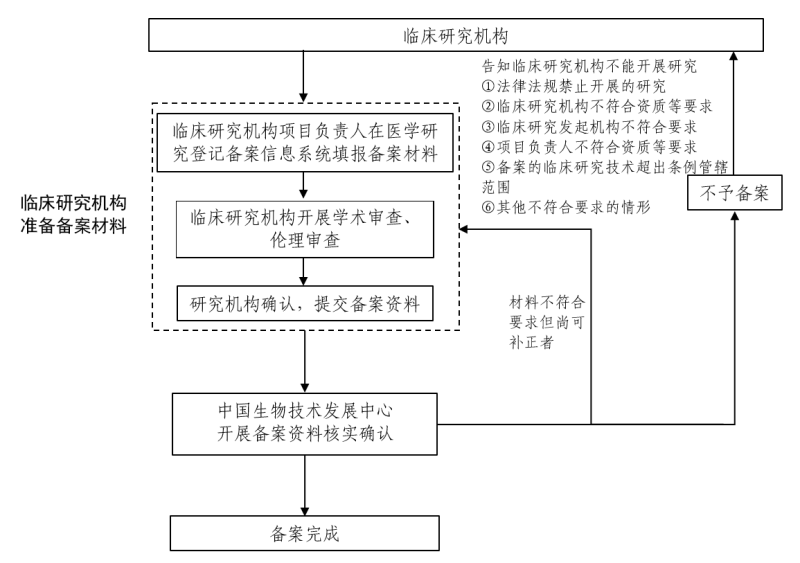
七、收费标准
无需收费
电子申报材料通过网上平台接收,平台网址:https://www.medicalresearch.org.cn/
(一)窗口咨询:国家卫生健康委行政审批受理窗口(生物中心办公区)
(二)电子邮件咨询:yxxjs@cncbd.org.cn
(三)电话咨询:010-88225109
(四)咨询时间:工作日8:30-11:30,13:30-16:30