日期:2026-05-01 来源:-- 供稿:现代医学与平台基地处 作者:-- 类别:摘录转发
生物医学新技术临床转化应用申报指南
一、基础信息
1.事项类型:行政许可
2.办件类型:承诺件
3.实施主体:中华人民共和国国家卫生健康委员会
4.行使层级:国家级
5.承诺办结时限:20个工作日(依法进行评估另需时间不计算在该时限内)
6.法定办结时限:20个工作日(依法进行评估另需时间不计算在该时限内)
7.是否收费:否
8.到办事现场次数:1次
9.咨询方式:
(一)窗口咨询:国家卫生健康委行政审批受理窗口(生物中心办公区),地址:北京市海淀区西四环中路16号院4号楼,中国生物技术发展中心;
(二)电话咨询:010-88225199;
(三)电子邮件咨询:yxxjs@cncbd.org.cn。
10.监督投诉方式:
(一)窗口投诉:国家食品安全风险评估中心纪检监察室(北京市朝阳区广渠路37号院2号楼);
(二)投诉电话:010-52165515;
(三)电子邮件投诉:jishenchu@cfsa.net.cn。
(四)信函投诉:国家食品安全风险评估中心纪检监察室(北京市朝阳区广渠路37号院2号楼),邮编100022。
11.办理时间:
办公时间:周一到周五:上午8:30-11:30,下午13:30-16:30,法定节假日按照国家规定执行。
12.办理地点:
国家卫生健康委行政审批受理窗口(生物中心办公区),地址:北京市海淀区西四环中路16号院4号楼,中国生物技术发展中心。
13.邮寄信息:
国家卫生健康委行政审批受理窗口(生物中心办公区),联系电话010-88225199,地址:北京市海淀区西四环中路16号院4号楼;邮编:100039。
二、办理流程
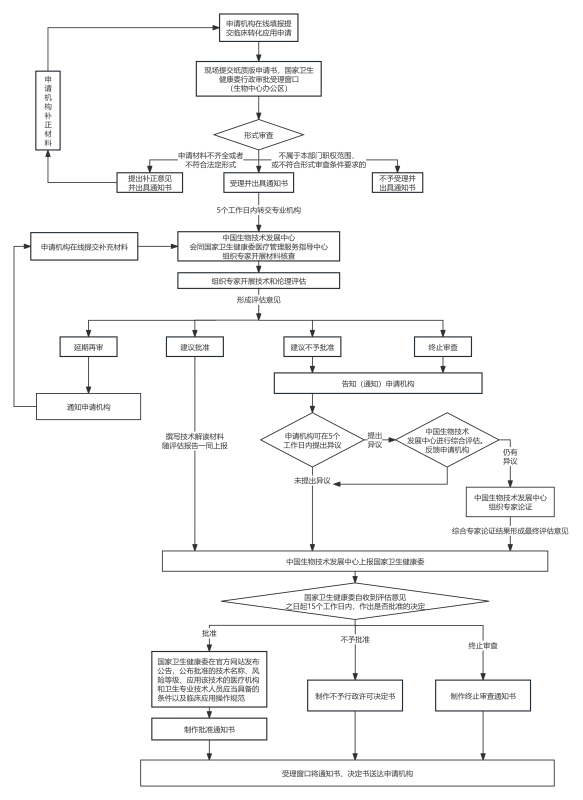
三、表格下载
四、受理条件
【审批范围】已列入《生物医学新技术临床研究备案指导清单》的生物医学新技术,满足下列要求之一的,纳入生物医学新技术临床转化应用审批范围:
(一)个性化程度高,国内尚没有使用同类机制原理的药品获得上市许可或者已启动确证性临床试验;
(二)用于治疗罕见病,国内尚没有使用同类机制原理、针对相同适应症的药品获得上市许可或者已启动确证性临床试验。
对符合《医疗器械监督管理条例》医疗器械定义的,应当按照医疗器械法规要求开展相关注册工作,不纳入生物医学新技术临床转化应用审批范围。
【申请条件】生物医学新技术申请临床转化应用,应当同时具备以下条件:
(一)经依法备案并完成生物医学新技术临床研究;
(二)生物医学新技术临床研究证明该技术安全、有效,符合伦理原则;
(三)在临床研究阶段,经多中心参与,遵守临床应用操作规范独立实施该技术,获得一致的安全性、有效性结论。
五、收费标准
无
六、设定依据
《生物医学新技术临床研究和临床转化应用管理条例》
七、实施依据
《生物医学新技术临床转化应用审批工作规范》